ВЕДЕНИЕ БЕРЕМЕННОСТИ
Пациентки с многоплодием должны посещать женскую консультацию чаще, чем при одноплодной: 2 раза в месяц до 28 нед (когда выдают листок нетрудоспособности по беременности и родам), после 28 нед — один раз в 7–10 дней. В течение беременности пациентки три раза должны посетить терапевта. Учитывая повышенную потребность в калорийности, белках, минералах, витаминах при многоплодной беременности особое внимание необходимо уделять вопросам полноценного сбалансированного питания беременной. Оптимальна при многоплодии, в отличие от одноплодной беременности, общая прибавка 20–22 кг. Беременным с многоплодием с 16–20 нед назначают противоанемическую терапию (оральный прием железосодержащих препаратов в дозе 60–100 мг/сутки и фолиевой кислоты — 1 мг/сутки в течение трёх месяцев). Для профилактики преждевременных родов беременным с многоплодием рекомендуют ограничение физической активности, увеличение продолжительности дневного отдыха (трижды по 1–2 ч). Расширяют показания к выдаче больничного листа. Для прогнозирования преждевременных родов необходимо исследовать состояние шейки матки. При этом методом выбора служит трансвагинальная цервикография, которая позволяет, помимо оценки длины шейки матки, определить состояние внутреннего зева, что невозможно при мануальном исследовании (рис. 213). Сроки гестации с 22–24 до 25– 27 нед — «критические» для беременных с многоплодием в отношении риска преждевременных родов. При длине шейки матки £34 мм в 22–24 нед повышен риск преждевременных родов до 36 недель; критерием риска преждевременных родов в 32–35 нед служит длина шейки матки £27 мм, а критерием риска «ранних» преждевременных родов (до 32 нед) — £19 мм.
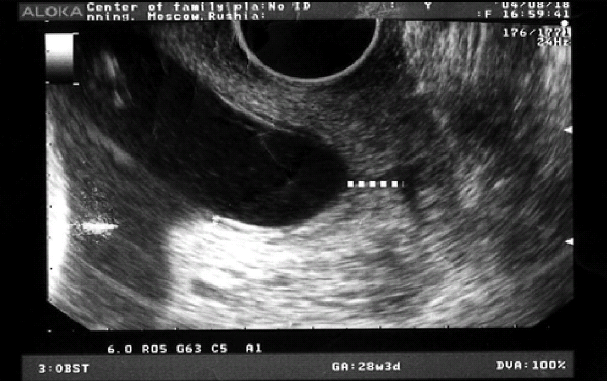
Рис. 21-3. Беременность 30 недель, двойня, резко укороченная шейка матки при угрозе преждевременных родов
(эхограмма).
Для ранней диагностики ЗРП необходим тщательный динамический ультразвуковой мониторинг. Для выработки тактики ведения беременности и родов, помимо фетометрии, при многоплодии так же, как и при одноплодной беременности, большое значение имеет оценка состояния плодов (КТГ, допплерометрия кровотока в системе матьплацентаплод, биофизический профиль). Существенное значение приобретает определение количества ОВ (много и маловодие) в обоих амнионах.
СПЕЦИФИЧЕСКИЕ ОСЛОЖНЕНИЯ МНОГОПЛОДНОЙ БЕРЕМЕННОСТИ. ТАКТИКА ВЕДЕНИЯ
При многоплодной беременности возможно развитие специфических, не характерных для одноплодной беременности, осложнений: СФФГ , обратная артериальная перфузия, внутриутробная гибель одного из плодов, ВПР одного из плодов, сросшиеся близнецы, хромосомная патология одного из плодов. СФФГ, впервые описанный Schatz в 1982 г., осложняет течение 5–25% многоплодных однояйцевых беременностей. ПС при СФФГ достигает 60–100% случаев. СФФГ(морфологический субстрат его — анастомозирующие сосуды между двумя фетальными системами кровообращения) — специфическое осложнение для монозиготной двойни с монохориальным типом плацентации, который наблюдают в 63–74% случаев однояйцевой многоплодной беременности. Вероятность возникновения анастомозов у монозиготных двоен с бихориальным типом плацентации не больше, чем у дизиготных двоен. Для СФФГ характерны артериовенозные анастомозы, расположенные не на поверхности, а в толще плаценты, которые практически всегда проходят через капиллярное ложе котиледона. Выраженность СФФГ (лёгкая, средняя, тяжёлая) зависит от степени перераспределения крови через эти анастомозы, которые варьируют в размерах, числе и направлении. Основным пусковым фактором развития СФФГ служит патология развития плаценты одного из плодов, который становится донором. Повышение периферической резистентности плацентарного кровотока приводит к шунтированию крови к другому плодуреципиенту. Таким образом, состояние плодадонора нарушается в результате гиповолемии, вследствие потери крови, и гипоксии на фоне плацентарной недостаточности. Плодреципиент компенсирует увеличение ОЦК полиурией. При этом увеличение коллоидного осмотического давления приводит к чрезмерному поступлению жидкости из материнского русла через плаценту. В результате этого состояние плодареципиента нарушается вследствие СН, обусловленной гиперволемией.
ДИАГНОСТИКА СИНДРОМА ФЕТОФЕТАЛЬНОЙ ГЕМОТРАНСФУЗИИ
Традиционно в течение многих лет диагноз СФФГ ставили ретроспективно в неонатальном периоде на основании разницы в содержании Hb (50 г/л и более) в периферической крови близнецов и различия в массе новорождённых (20% и более). Однако значительная разница в уровне Hb и массе новорождённых характерна и для некоторых бихориальных двоен, в связи с чем в последние годы эти показатели перестали рассматривать как признаки СФФГ. На основании ультразвуковых критериев разработаны стадии СФФГ (Quintero R. et al, 1999), которые используют в практике для определения тактики ведения беременности:
I стадия: мочевой пузырь плодадонора определяется;
II стадия: мочевой пузырь плодадонора не определяется, состояние кровотока (в артерии пуповины и/или венозном
протоке) некритическое;
III стадия: критическое состояние кровотока (в артерии пуповины и/или венозном протоке) у плодадонора и/или
реципиента;
IV стадия: водянка у плодареципиента;
V стадия: антенатальная гибель одного или обоих плодов.
Патогномоничными эхографическими признаками тяжёлого СФФГ служат: наличие большого мочевого пузыря у плодареципиента с полиурией на фоне выраженного многоводия и «отсутствие» мочевого пузыря у плодадонора с анурией, для которого характерно снижение двигательной активности на фоне выраженного маловодия.
Метод выбора в лечении СФФГ тяжёлой степени — лазерная коагуляция анастомозирующих сосудов плаценты под эхографическим контролем, так называемая соноэндоскопическая техника. Эффективность эндоскопической лазеркоагуляционной терапии СФФГ (рождение хотя бы одного живого ребёнка) составляет 70%. Этот метод предполагает трансабдоминальное введение фетоскопа в амниотическую полость плодареципиента. Комбинация ультразвукового наблюдения и непосредственного визуального осмотра через фетоскоп позволяет осуществлять обследование хорионической пластины вдоль всей межплодовой перегородки, выявить и произвести коагуляцию анастомозирующих сосудов. Оперативное вмешательство заканчивают дренированием ОВ до нормализации их количества. С помощью эндоскопической лазерной коагуляции возможно пролонгирование беременности в среднем на 14 нед, что приводит к снижению внутриутробной гибели плодов с 90 до 29%. Альтернативной тактикой ведения беременных с выраженным СФФГ при отсутствии возможности проведения лазерной коагуляции анастомозирующих сосудов плаценты служит дренирование избыточного количества АЖ из амниотической полости плодареципиента. Этот паллиативный метод лечения, который можно применять неоднократно в динамике беременности, не устраняет причину СФФГ, однако способствует снижению внутриамниотического давления и тем самым компрессии, как правило, оболочечно прикреплённой пуповины и поверхностных сосудов плаценты, что в определённой мере улучшает состояние как плодадонора, так и плода- реципиента. К положительным эффектам амниодренирования следует отнести и пролонгирование беременности как следствие снижения внутриматочного объёма. Эффективность амниодренажа, проводимого под контролем УЗИ, составляет 30–83%. Основная и наиболее важная разница в перинатальных исходах при проведении эндоскопической лазеркоагуляции и повторных амниодренажей состоит в частоте неврологических нарушений у выживших детей (5% против 18–37% соответственно). Обратная артериальная перфузия у двоен — патология, присущая только монохориальной беременности (наиболее выраженное проявление СФФГ). В основе этой патологии лежит нарушение сосудистой перфузии, в результате чего один плод (реципиент) развивается за счёт плодадонора вследствие наличия пупочных артериоартериальных анастомозов. При этом у плодадонора («насоса»), как правило, не бывает структурных аномалий, но могут быть признаки водянки. Плодреципиент («паразитирующий») всегда с множественными аномалиями, несовместимыми с жизнью: могут отсутствовать голова и сердце (или значительные дефекты этих органов, например рудиментарное сердце). Прогноз для плодадонора также неблагоприятен: при отсутствии внутриутробной коррекции смертность достигает 50%. Единственная возможность сохранить жизнь плодудонору — фетоцид плодареципиента (лигирование пуповины).
Внутриутробная гибель одного из плодов при многоплодной беременности может наблюдаться в любом сроке гестации и результатом этого может быть «отмирание» одного плодного яйца в I триместре, что отмечают в 20% наблюдений, и «бумажный плод» во II триместре беременности. Средняя частота гибели одного или обоих плодов на ранних сроках гестации составляет 5% (2% при одноплодной беременности). Частота поздней (во II и III триместрах беременности) внутриутробной гибели одного из плодов составляет 0,5–6,8% при двойне и 11,0–17,0% при тройне. Основные причины поздней внутриутробной гибели при монохориальной плацентации — СФФГ, а при бихориальной — ЗРП и оболочечное прикрепление пуповины. При этом частота внутриутробной гибели плода при монохориальной двойне в 2 раза превышает таковую при бихориальной многоплодной беременности. При гибели одного из плодов в I триместре беременности в 24% наблюдений может погибнуть и второй или происходит самопроизвольный аборт, однако в большинстве наблюдений возможно отсутствие какихлибо неблагоприятных последствий для развития второго плода. При гибели одного из плодов во II–III триместрах беременности возможно преждевременное прерывание беременности вследствие выделения «мёртвой» плацентой цитокинов и ПГ. Огромный риск для выжившего плода представляют и повреждения головного мозга, что обусловлено выраженной гипотензией вследствие перераспределения крови («кровотечения») от живого плода в фетоплацентарный комплекс погибшего. При внутриутробной гибели одного из плодов при бихориальной двойне оптимальным считают пролонгирование беременности (рис. 214). При монохориальном типе плацентации единственный выход для спасения жизнеспособного
плода — КС, произведённое как можно быстрее после гибели одного из плодов, когда ещё не произошло повреждение головного мозга выжившего плода. При внутриутробной гибели одного из плодов из монохориальной двойни на более ранних сроках (до достижения жизнеспособности) методом выбора служит немедленная окклюзия пуповины мёртвого плода.
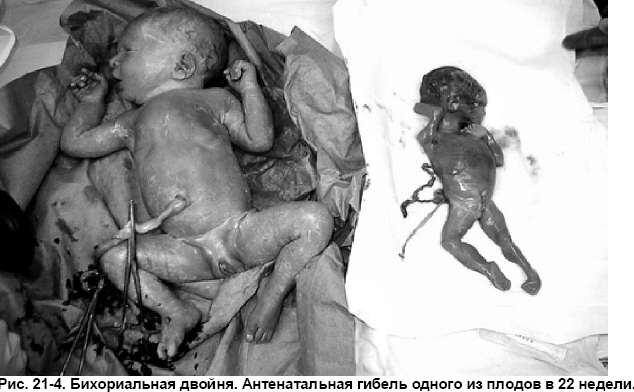
Рис. 21-4. Бихориальная двойня. Антенатальная гибель одного из плодов в 22 недели.
Тактика ведения многоплодной беременности, дискордантной в отношении ВПР плода, зависит от степени выраженности порока, гестационного возраста плода на момент диагностики и, что особенно важно, типа плацентации. При бихориальной двойне возможен селективный фетоцид больного плода (внутрисердечное введение раствора калия хлорида под контролем УЗИ), однако, учитывая небезопасность проводимой инвазивной процедуры, при абсолютной летальности порока (например, анэнцефалии) следует рассматривать вопрос и о выжидательной тактике с целью снижения риска проводимой процедуры для второго плода. При монохориальной плацентации наличие межплодовых трансплацентарных анастомозов исключает возможность селективного фетоцида с использованием раствора калия хлорида ввиду опасности его попадания погибшего плода живому. При монохориальной двойне используют другие методы фетоцида больного плода: инъекция чистого алкоголя во внутрибрюшную часть пупочной артерии, перевязка пуповины при фетоскопии, эндоскопическая лазерная коагуляция, введение под эхографическим контролем тромбогенной спирали, эмболизация больного плода. Оптимальной тактикой ведения монохориальной двойни при дискордантности в отношении ВПР считают окклюзию сосудов пуповины больного плода (рис. 215).
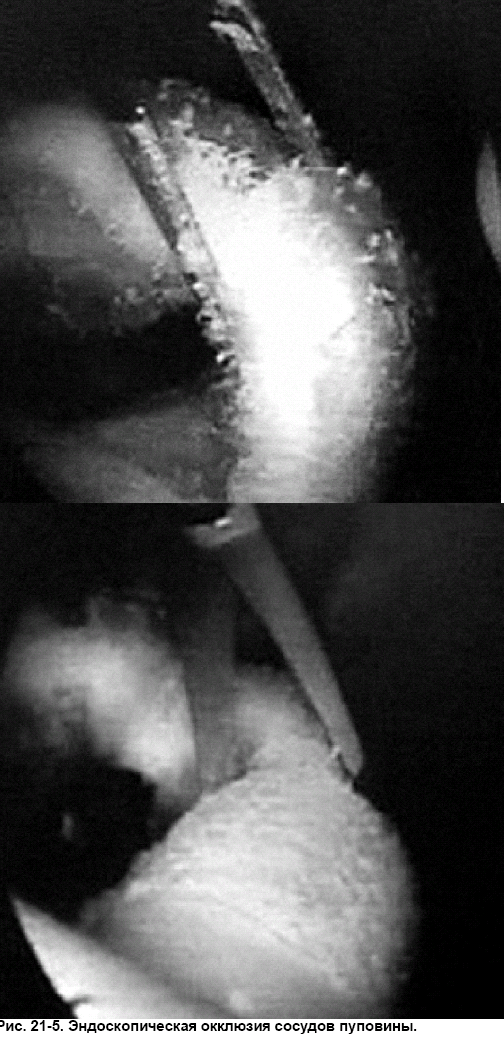
Сросшиеся близнецы — специфический порок развития, характерный для монохориальной моноамниотической беременности. Это редкая патология, частота которой составляет 1% монохориальных двоен. К наиболее частым типам срастания относят: торакопаги (сращение в области грудной клетки), омфалопаги (сращение в области пупка и хряща мечевидного отростка), краниопаги (сращение гомологичными частями черепа), пигопаги и ишиопаги (соединение боковых и нижних отделов копчика и крестца), а также неполное расхождение (раздвоение только в одной части тела). Прогноз для сросшихся близнецов зависит от места, степени соединения и от наличия сопутствующих пороков развития. В связи с этим для более точного установления потенциальной возможности выживания детей и их разделения, помимо УЗИ, необходимы такие дополнительные методы исследования, как эхокардиография и МРТ. При внутриутробно диагностированной (в ранние сроки) сросшейся двойне беременность прерывают. При возможности хирургического разделения новорождённых и согласии матери выбирают выжидательную тактику при ведении такой беременности. Хромосомную патологию при двуяйцевой многоплодной беременности (у каждого плода) наблюдают с такой же частотой, как при одноплодной, при этом возможность поражения по меньшей мере одного из плодов удваивается. У однояйцевых двоен риск хромосомной патологии такой же, как и при одноплодной беременности, и в большинстве наблюдений поражаются оба плода. Если тактика ведения беременных с двойней при диагностированной трисомии обоих плодов однозначна — прерывание беременности, то при дискордантности плодов в отношении хромосомной патологии возможны или селективный фетоцид больного плода, или пролонгирование беременности без какоголибо вмешательства. Тактика полностью основана на относительном риске селективного фетоцида, который может стать причиной выкидыша, преждевременных родов, а также гибели здорового плода. Вопрос о пролонгировании беременности с вынашиванием заведомо больного ребёнка нужно решать с учётом желания беременной и её семьи.
Перейти на страницу 2
Читайте также Многоплодная беременность
