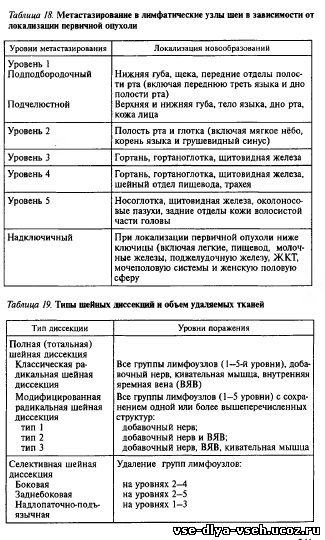
Рак губы и слизистой оболочки полости рта
Рак органов полости рта развивается в 5—7 раз чаще у мужчин, чем у женщин. Соотношение мужчины/женщины — 3:1.Обычно чаще болеют люди в возрасте 60—70 лет. Заболеваемость увеличивается после 40 лет и уменьшается в возрасте 80 лет. Однако в последние годы частота возникновения рака полости рта в возрастной группе 30—40 лет возросла. Ежегодно в Беларуси регистрируется около 130 случаев рака дна полости рта. Число злокачественных опухолей дна полости рта составляет около 10—15% от общего количества опухолей, локализованных в полости рта.
Этиология и факторы риска. Как и в отношении всех других опухолей головы и шеи, существует прямая зависимость между курением и возникновением злокачественных опухолей в полости рта. Выявлена корреляция между количеством выкуриваемых сигарет и развитием злокачественных опухолей. Более 90% больных раком, локализующимся в полости рта, курят и многие из них употребляют алкоголь. Неумеренное употребление алкоголя само по себе является фактором риска развития опухолей полости рта (хотя алкоголь в меньшей степени канцероген, чем табак). Для употребляющих одновременно табак и алкоголь эти факторы риска будут синергичными и приведут к значительному увеличению риска возникновения рака полости рта. У излеченных больных, продолжающих курить, риск развития рецидива рака полости рта составляет 40—60%.Пациенты с дефицитом витамина А входят в группу повышенного риска, в то время как диета, богатая фруктами и овощами, оказывает защитный эффект в отношении возникновения злокачественных опухолей в полости рта. Хроническая механическая травма, вызванная разрушенной коронкой зуба, острым краем пломбы или некачественно изготовленным зубным протезом, а также несоблюдение гигиены полости рта способствуют развитию опухолей. Несомненно и вредное влияние систематического употребления слишком горячей и острой пищи. Выявлено, что вирусы Herpes simplex I типа и папил- ломавирус человека вовлечены в процесс развития опухолей полости рта.
Предраковые заболевания. Лейкоплакия является результатом хронического повреждения слизистых мембран канцерогенами. Это повреждение стимулирует пролиферацию эпителиальной и соединительной ткани. Гистопатологическое обследование обнаруживает гиперкератоз, связанный с подлежащей эпителиальной гиперплазией. При отсутствии подлежащей дисплазии, лейкоплакия редко (менее 5%) малигнизируется.Эритроплакия характеризуется поверхностными, рыхлыми, красными пятнами, прилежащими к нормальной слизистой оболочке. Это обычно встречается с подлежащей эпителиальной дисплазией и имеет гораздо больший потенциал малигнизации,чем лейкоплакия. Около 40% эритроплакий малигнизируются.
Дисплазия характеризуется клеточной атипией, потерей нормального созревания и эпителиального расслоения. Она поделена на степени: низкую, среднюю и высокую, в зависимости от имеющейся атипии ядер. При переходе от низкой к высокой степени дисплазии атипия ядер становится более четкой, митозы — более видимыми. Эти изменения затрагивают все большую толщину эпителия. Вероятность развития карциномы основана на степени дисплазии. В случае высокой степени дисплазии приблизительно у 24% больных может развиться инвазивный плоскоклеточный рак.
Классификация. В настоящее время применимы ΤΝΜ-классификация и гистологическая классификация.
ΤΝΜ-классификация
Анатомические области и части:
Губа
1. Верхняя губа, красная кайма (С00.0).
2. Нижняя губа, красная кайма (С00.1).
3. Углы рта (комиссуры) (С00.6).
Полость рта
4. Слизистая оболочка:
a) слизистая оболочка верхней и нижней губ (СОО.3,4);
b) слизистая оболочка щек (С06.0);
c) ретромолярная часть (С06.2);
d) щечно-альвеолярные складки (борозды), верхняя и нижняя
(преддверие рта) (С06.1).
5. Верхний альвеолярный отросток и десна (С03.0).
6. Нижний альвеолярный отросток и десна (С03.1).
7. Твердое нёбо (С05.0).
8. Язык:
a) спинка и боковые края кпереди от валикообразных сосочков
(передние две трети) (С02.0,1);
b) нижняя поверхность (С02.2).
9. Дно полости рта (С04).
Примечание. Корень языка (С01.9) относится к глотке.
Т — первичная опухоль
ТХ — недостаточно данных для оценки первичной опухоли.
ТО — первичная опухоль не определяется.
Tis — преинвазивная карцинома (carcinoma in situ).
T1 — опухоль до 2 см в наибольшем измерении.
Т2 — опухоль до 4 см в наибольшем измерении.
ТЗ — опухоль более 4 см в наибольшем измерении.
Т4а — опухоль прорастает кортикальную пластинку нижней челюсти, кожу.
Т4Ь —опухоль прорастает в крылонёбную ямку, боковую стенку глотки, основание черепа или вовлекает в процесс внутреннюю сонную артерию.
Примечания. 1. К глубоким мышцам языка относятся: подъязычно-язычная мышца, шилоязычная мышца, подбородочно-язычная мышца,нёбно-язычная мышца.
2. Поверхностной эрозии костно-зубной впадины первичной опухолью десны недостаточно для обозначения процесса как Т4.
3. В случаях, когда имеются сомнения в распространении опухоли на кость, руководствуются параграфом 4 общих правил системы ΊΓΝΜ: «Если имеются сомнения в правильности определения категорий Т, N или М, то надо выбирать низшую (т.е. менее распространенную) категорию».
Если при сцинтиграфии определяется очаг патологически повышенного накопления радиофармпрепарата, то опухоль относится к категории Т4.
N — регионарные лимфатические узлы
1-й уровень — лимфатические узлы подбородочного и подчелюстного треугольников.
2-й уровень — верхняя яремная цепочка лимфатических узлов,распространяющаяся от нижней челюсти вниз до бифуркации сонных артерий и кзади до задней границы грудино-ключично-сосцевидной мышцы.
3-й уровень — яремные лимфатические узлы от каротидного сосудистого пучка до лопаточно-подчелюстной мышцы.
4-й уровень — лимфатические узлы от лопаточно-подчелюстной мышцы вниз до ключицы.
5-й уровень — лимфатические узлы заднего треугольника, ограниченного спереди задним краем грудино-ключичнососцевидной мышцы, сзади — передним краем трапециевидной мышцы и снизу — ключицей.
Первым эшелоном лимфатических узлов для опухолей губы и слизистой оболочки полости рта являются подподбородочные, подчелюстные, верхние и средние яремные узлы.
NX — недостаточно данных для оценки состояния регионарных лимфатических узлов.
N0 — нет признаков метастатического поражения регионарных лимфатических узлов.
N 1 — метастазы в одном лимфатическом узле на стороне поражения до 3 см и менее в наибольшем измерении.
N2 — метастазы в одном или нескольких лимфатических узлах на стороне поражения более чем 3 см, но менее 6 см в наибольшем измерении или метастазы в лимфатических узлах шеи с обеих сторон, или с противоположной стороны до 6 см в наибольшем измерении.
N2a — метастазы в одном лимфатическом узле на стороне поражения до 6 см в наибольшем измерении.
,N2b — метастазы в нескольких лимфатических узлах на стороне поражения до 6 см в наибольшем измерении.
N2c — метастазы в лимфатических узлах с обеих сторон или с противоположной стороны до 6 см в наибольшем измерении.
N3 — метастаз в лимфатическом узле более 6 см в наибольшем измерении.
М — отдаленные метастазы
MX — недостаточно данных для определения отдаленных метастазов.
МО — нет признаков отдаленных метастазов.
Μ1 — имеются отдаленные метастазы
Патогистологическая классификация
Требования к определению категорий рТ, pN и рМ соответствуют таковым к определению категорий Т, N и М.
G — гистопатологическая дифференцировки
GX — степень дифференцировки не может быть установлена.
G1 — высокая степень дифференцировки.
G2 — средняя степень дифференцировки.
G3 — низкая степень дифференцировки.
G4 — недифференцированные опухоли.
Группировка по стадиям
I стадия Т1 N0 МО
II стадия Т2 N0 МО
III стадия ТЗ N0 МО
Т1 N1 МО
Т2 N1 МО
ТЗ N1 МО
IV А с т а д и я Т1 N2 МО
Т2 N2 МО
ТЗ N2 МО
Т4а N0 МО
Т4а N1 МО
Т4а N2 МО
Т4Ь Любая N МО
Любая Т N3 МО
Любая Т Любая N Ml
IV В стадия
IV С стадия
R-классификация
Наличие или отсутствие остаточной опухоли после лечения обозначается символом R. Определения R-классификации применимы ко всем локализациям опухолей головы и шеи. Эти определения следующие:
RX — наличие остаточной опухоли не определяется.
R0 — остаточной опухоли нет.
R1 — микроскопическая остаточная опухоль.
R2 — макроскопическая остаточная опухоль.
Диагностика. Проводятся следующие диагностические мероприятия:
• орофарингоскопия и ларингоскопия;
• бимануальная пальпация губы, языка, щек, тканей дна полости рта, пальпаторное исследование миндалин;
• пальпаторное обследование лимфатических узлов шеи с обеих сторон (при клинически неопределяемых метастазах в лимфатические узлы — УЗИ шеи);
• рентгенологическое исследование органов грудной клетки;
• ортопантомография нижней и верхней челюсти (при подозрении на вовлечение в опухоль костных структур);
• компьютерная рентгенотомография головы и шеи (при невозможности установления распространенности опухоли другими методами исследования);
• компьютерная рентгенотомография — ангиография (выполняется при планировании хирургического вмешательства на шее у больных с подозрением на вовлечение в опухолевый процесс крупных магистральных сосудов);
• морфологическая верификация опухоли с установлением
гистологического типа и степени дифференцировки опухоли (инцизионная биопсия);
• цитологическая верификация опухоли (не исключает гистологической верификации) и регионарных лимфогенных метастазов;• эзофагогастро- и бронхоскопия (при наличии жалоб).
Лабораторные исследования:
• общий анализ крови;
• определение группы крови и Rh-фактора;
• биохимический анализ крови (общий белок, креатинин, мочевина, билирубин, щелочная фосфатаза, ионы — Na+, К+,Са2+, С1- , глюкоза);
• клиренс креатинина (при планировании химиотерапии);
• коагулограмма (по показаниям и на этапе предоперационной подготовки);
• ЭКГ;
• Эхо-КГ (при планировании химиотерапии);
• общий анализ мочи.
Лечение. Лечение органосохранное.
Хирургический метод. Среди хирургических подходов при первичном раке применяются внутриротовые, трансцервикальные и комбинированные операции. Небольшие опухоли удаляются через рот. При удалении распространенных опухолей выполняют моноблочные комбинированные резекции с интраоперационным контролем радикальности выполненного хирургического вмешательства. При локализации опухоли в задних отделах полости рта возможно удаление опухоли после рассечения нижней челюсти. При этом отдается предпочтение медиальной мандибулотомии.
При вторичном поражении нижней челюсти лечение комплексное.
Лучевое лечение. Результаты лучевого лечения больных с опухолями губы и слизистой оболочки полости рта I—II стадии в целом сопоставимы с таковыми при хирургическом и комбинированном методах. Применяются короткофокусная рентгенотерапия и электротерапия (только для рака губы), телегамматерапия и сочетанная лучевая терапия.
При проведении сочетанной лучевой терапии между завершением дистанционного облучения и проведением контактной лучевой терапии интервал составляет 7—10 дней (если этот интервал более длителен, то продолжается дистанционная лучевая терапия). В случае четко отграниченных поверхностных опухолей ΤΙ—Т2 без регионарных метастазов методом выбора является брахитерапия.
Распространенные опухоли (ТЗ—Т4) лечат с использованием лучевой терапии в виде предоперационного и (или) послеоперационного воздействия с целью создания более благоприятных условий для радикального хирургического вмешательства и уменьшения числа рецидивов. В настоящее время наиболее обоснованным является послеоперационная лучевая терапия, позволяющая, не увеличивая числа послеоперационных осложнений существенно снизить частоту развития местных рецидивов. Тем не менее, проведение предоперационной лучевой терапии может быть обоснованным при местно-распространенных опухолях на грани резектабельности или несмещаемых метастазах в лимфатических узлах (СОД — 46—50 Гр, РОД - 2 Гр). Кроме того, предоперационную лучевую терапию можно
проводить у соматически ослабленных больных с резектабельными опухолями, используя этот период для общеукрепляющего лечения и подготовки к операции.
При профилактическом или лечебном облучении регионарного лимфатического коллектора в планируемый объем облучения включаются лимфатические узлы шеи со стороны поражения, а при центральной локализации опухоли — лимфатические узлы шеи с обеих сторон. Облучение регионарных лимфатических узлов проводится параллельно с лучевой терапией первичной опухоли или в рамках послеоперационной лучевой терапии.
Показанием к проведению послеоперационной лучевой терапии являются:
• опухоли ТЗ—Т4;
• резидуальная опухоль;
• периневральная, лимфатическая, сосудистая инвазии;
• шейная лимфодиссекция по поводу множественных метастазов или их экстракапсулярного распространения.
В качестве основного метода лечения лучевая терапия также применяется при нерезектабельных опухолях или высоком операционном риске.
Химиолучевое лечение. Химиолучевое лечение у больных с резектабельными опухолями губы и слизистой оболочки полости рта в стандартных ситуациях используется в послеоперационном периоде при морфологическом подтверждении наличия опухоли в крае отсечения (если невозможна реоперация), а также при наличии периневральной, лимфатической, сосудистой инвазий, после лимфодиссекции по поводу множественных регионарных метастазов (N2, N3).
Показаниями к применению этого лечения в предоперационном периоде у больных с резектабельными опухолями являются местно-распространенные опухоли или несмещаемые метастазы, возможность радикального удаления которых вызывает сомнение.Операции на регионарном лимфаденаппарате. Шейная лимфодиссекция выполняется при наличии метастатического поражения
лимфатических узлов, неполной регрессии метастазов после облучения или с профилактической целью (селективная лимфодиссекция).
Если лечение начинается с хирургического вмешательства, шейная лимфодиссекция выполняется одновременно с удалением первичной опухоли. При двустороннем метастатическом поражении лимфатических узлов (рис. 21) шейная лимфодиссекция выполняется с обеих сторон поочередно с интервалом в 2—3 недели (табл. 18, 19).
Радикальная шейная лимфодиссекция выполняется при множественных смещаемых метастазах или одиночных, но ограниченно смещаемых, спаянных со внутренней яремной веной и грудино-ключично-сосцевидной мышцей. Модифицированные радикальные шейные лимфодиссекции производятся при одиночных, смещаемых, не спаянных с соседними анатомическими структурами шеи метастазами в
шейных лимфатических узлах. Селективные лимфодиссекции могут выполняться у пациентов с клинически не определяемыми шейными метастазами (N0).
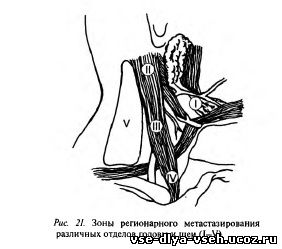
Рис. 21. Зоны регионарного метастазированияразличных отделов головы и шеи (I—V)
Рак языка. В передних 2/3 языка локализуется 75% всех злокачественных опухолей языка. Соотношение мужчины/женщины — 3:1. Возраст больных составляет в среднем 60 лет, но рак языка может возникать и у больных моложе 30 лет.Наиболее частыми симптомами у больных раком языка являются боль, затруднение при глотании и разговоре. Злокачественные опухоли языка растут обычно инфильтративно и быстрее, чем раки других локализаций в полости рта. При этом более важной является глубина прорастания, а не площадь инфильтрата. Метастазы в лимфатических узлах шеи при раке языка обнаруживаются у 40% больных. При опухолях боковой поверхности тела языка двусторонние и контралатеральные метастазы наблюдаются редко. При лечении рака языка необходимо принимать во внимание агрессивность опухолей данной локализации и высокой вероятности скрытого лимфогенного, в том числе билатерального, метастазирования. Хирургический метод лечения применим лишь для I стадии рака подвижной части языка. Лучевая терапия в качестве единственного метод лечения может использоваться при опухолях ΤΙ—Т2 с минимальной инфильтрацией подлежащих тканей и без распространения на альвеолярный отросток челюсти. Основной метод лечения рака языка — комбинированный. В стандартных ситуациях хирургическое вмешательство выполняется на первом этапе. Послеоперационное облучение начинают сразу после заживления раны. Проведение предоперационной лучевой терапии (СОД — 46—50 Гр, РОД — 2 Гр) при резектабельных опухолях не является
оптимальной тактикой, но ее проведение возможно. Она может быть использована в ряде случаев у больных с местно-распространенными опухолями на грани резектабельности или несмещаемых метастазах в лимфатических узлах, а также у соматически ослабленных больных (с одновременным проведением общеукрепляющего лечения и подготовки к операции).Операция выполняется через 2—3 недели после завершения лучевой терапии.При всех стадиях в рамках радикального лечения проводится облучение лимфатических узлов шеи (1—4-й уровни) или выполняется шейная лимфодиссекция. Частота излеченности после лучевой терапии или хирургического вмешательства примерно одинакова для опухолей в стадии ΤΙ (80%) и Т2 (60%), а при ТЗ—Т4 после комбинированного и комплексного лечения она составляет 15—35%. Наличие метастазов в лимфатических узлах уменьшает показатель выживаемости на 50%.Рак слизистой оболочки дна полости рта. Злокачественные новообразования дна полости рта составляют около 10—15% отвсех опухолей полости рта.
Соотношение мужчины/женщины — 3:1. Средний возраст пациентов — 60 лет. Начало заболевания обычно бессимптомно. Поэтому обращение к врачу с жалобами на появление болезненного образования под языком является признаком прорастания опухоли вглубь тканей. Фиксация опухоли к кости свидетельствует о возможности вовлечения нижней челюсти в опухолевый процесс.
Ортопантомография нижней челюсти позволяет выявить инвазию в нижнюю челюсть. Ограниченная подвижность языка является признаком инвазивного роста опухоли в кореньязыка. В подобных случаях пальпация тканей дна полости рта часто дает больше информации о глубине инвазивного роста, чем простой осмотр. Опухоли, локализованные в передних отделах рта около средней линии, могут обтурировать проток подчелюстной и подъязычной слюнных желез, что приводит к их воспалению и увеличению. В такой ситуации трудно отличить подчелюстную слюнную железу от метастазов в лимфатических узлах. Небольшие опухоли (Т1 и Т2) могут быть излечены путем широкого хирургического иссечения или при помощи лучевой терапии. Хирургический метод можно использовать при ограниченных поверхностных опухолях передних отделов полости рта или при вторичном поражении кости небольшой по размерам опухолью слизистой оболочки. При распространенном опухолевом процессе (ТЗ—Т4) проводится комбинированное лечение (операция + лучевая терапия). Показания к предоперационной лучевой терапии ограничены. Во всех случаях проводится профилактическое или лечебное облучение лимфатических узлов шеи.
Рак губы. Показатель заболеваемости злокачественными новообразованиями губы в Республике Беларусь составил 1,6 на 100 000 жителей в 2003 г. и 1,8 на 100 000 жителей в 2004 г.
Соотношение мужчины/женщины — 3:1.У больных раком губы широко используются лучевая, хи- миолучевая терапия и хирургическое вмешательство. Применение дистанционной лучевой терапии на зону лимфатических узлов шеи в суммарной дозе 50—70 Гр и сочетанной (дистанционной и брахитерапии) на первичный очаг в СОД 60—80 Гр позволяет при ранних стадиях заболевания (ΤΙ—Т2) достигнуть регрессии опухоли в 90—100% случаев. Хирургическое лечение при ΤΙ—Т2 включает в себя блоковую резекцию с отступом от края видимой опухоли не менее 1,5 см. Образовавшийся дефект замещается, как правило, местными тканями, методика зависит от локализации и величины дефекта. Выбор метода лечения (хирургический или лучевая терапия) зависит от ожидаемых функциональных и косметических результатов, подготовленности хирургов и наличия аппаратуры для проведения лучевой терапии. При злокачественных опухолях, соответствующих ТЗ—Т4, проводится комплексное лечение, включающее неоадъювантную химиотерапию, предоперационную лучевую терапию, хирургическое лечение и послеоперационную лучевую терапию в суммарной дозе 70 Гр. Среди хирургических подходов при первичном раке применяются комбинированные операции, в том числе с использованием лоскутов с осевым типом кровообращения. При лучевой терапии обычно используются два противолежащих поля. Запас в 1—2 см нормальных тканей должен быть запланирован всегда. У больных раком губы без клинически определяемых метастазов рекомендуется примененять брахи- терапию. Однако общая доза и общее время лечения должны строго соблюдаться. Между завершением дистанционного облучения и проведением контактной лучевой терапии интервал составляет 7—10 дней (если этот интервал более продолжителен, контактная лучевая терапия не проводится). В планируемый объем облучения включаются все лимфатические узлы шеи со стороны поражения, а при центральной локализации опухоли — лимфатические узлы шеи с обеих сторон. Диссекция лимфатических узлов шеи показана больным с не полностью регрессировавшими после облучения пальпируемыми шейными метастазами. При необходимости она выполняется с обеих сторон шеи, но поочередно.
